A veces, los hallazgos más interesantes en ecografía aparecen cuando menos los esperamos.
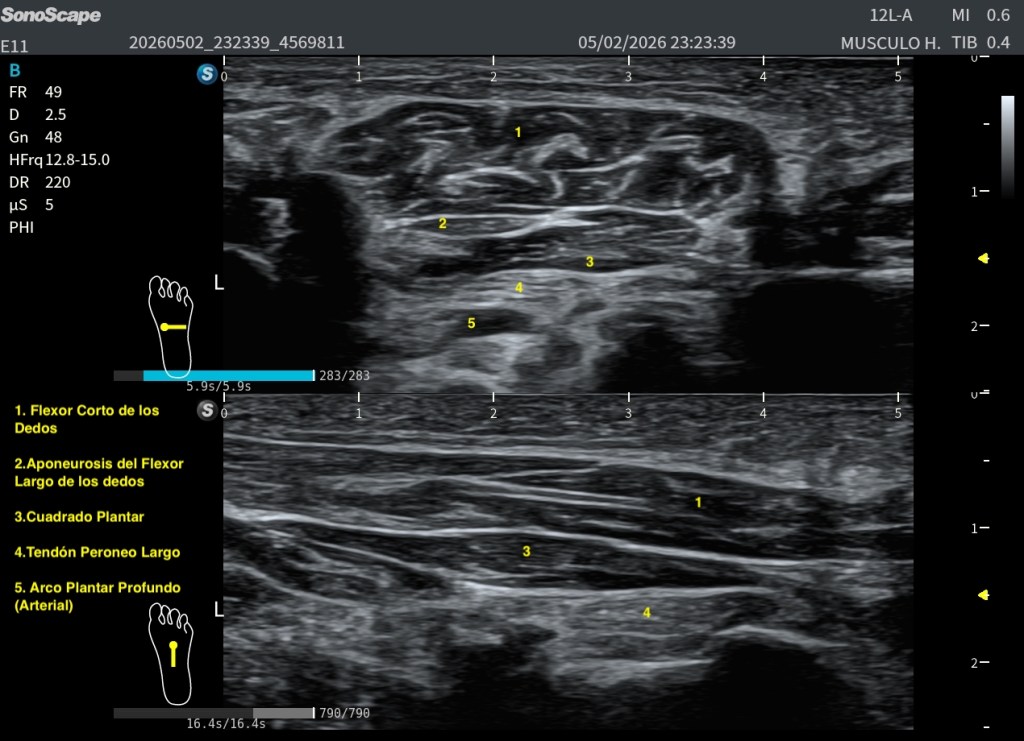
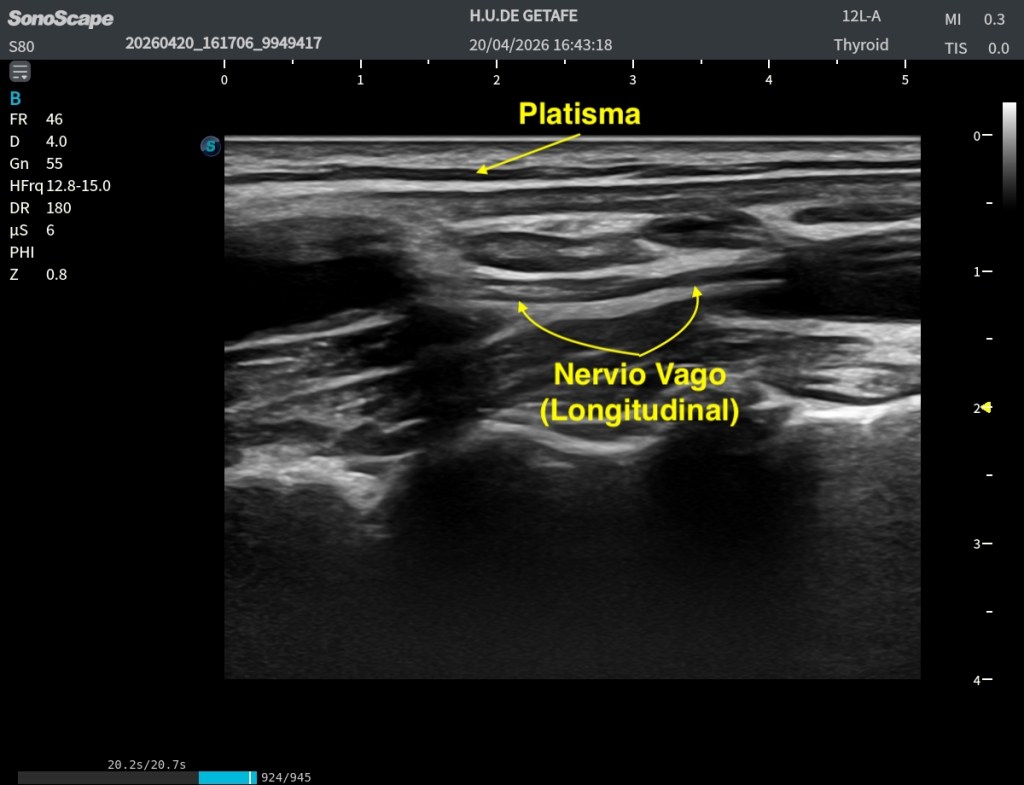
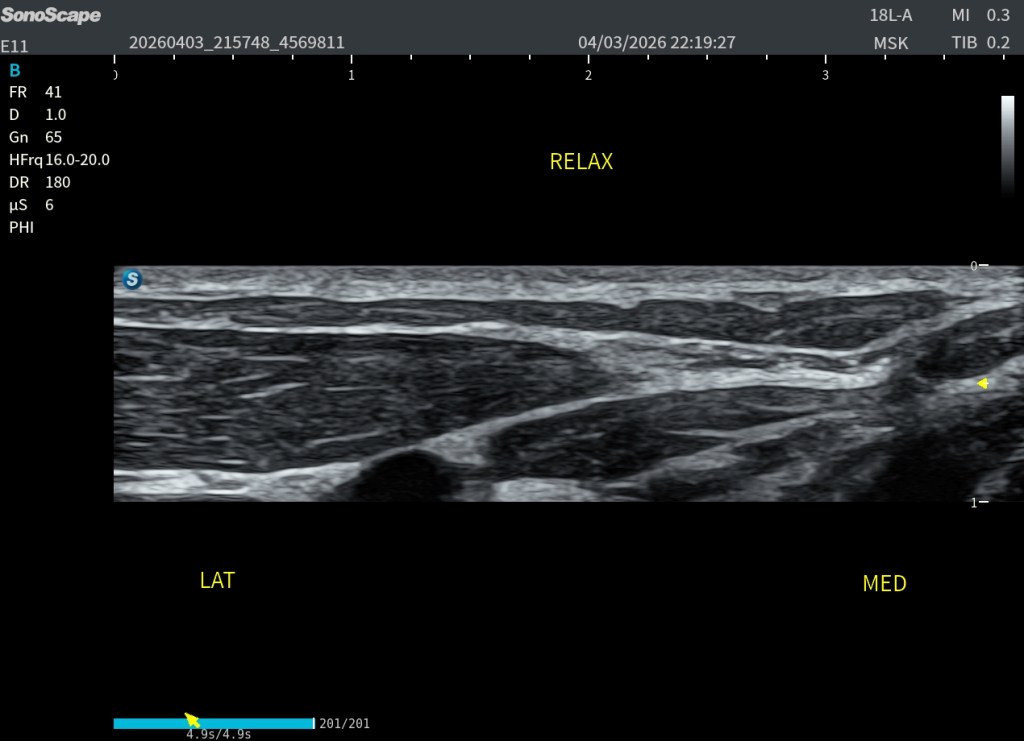
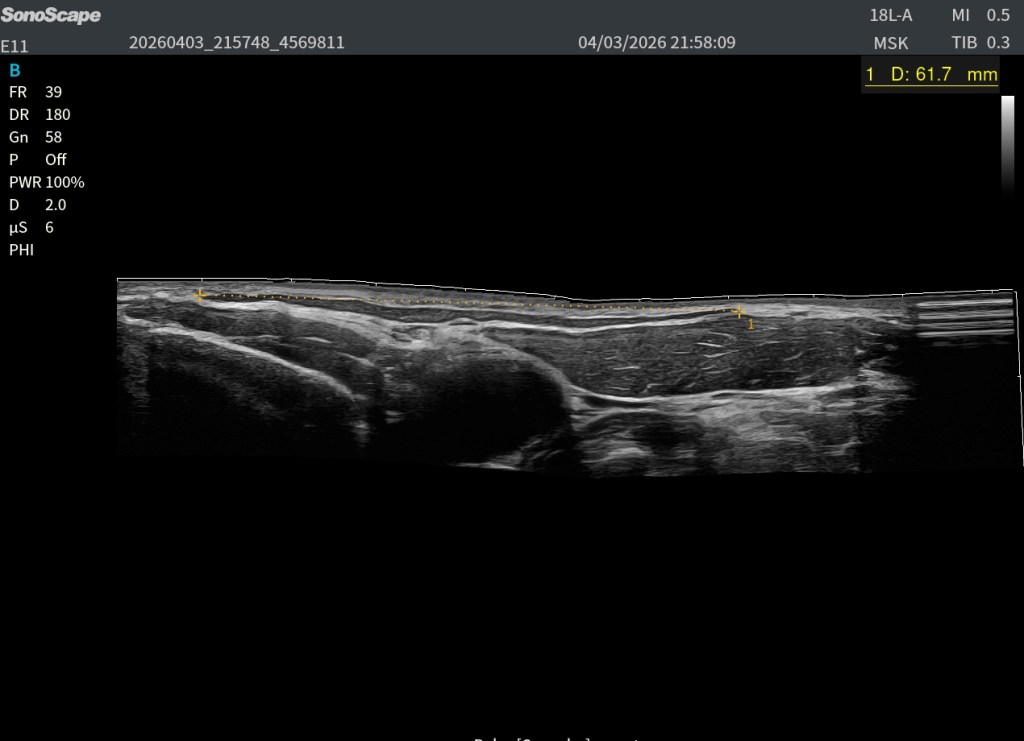
Durante una exploración ecográfica que no estaba orientada al estudio de una lesión muscular, apareció de forma casual una imagen intramuscular llamativa. En el modo B se identificaba una estructura claramente hiperecogénica localizada en el espesor muscular, visible tanto en el corte axial (transversal) como en el corte longitudinal. Precisamente en este último plano, la lesión alcanzaba aproximadamente 47 mm de longitud, situándose en una región compatible con una unión miofascial.
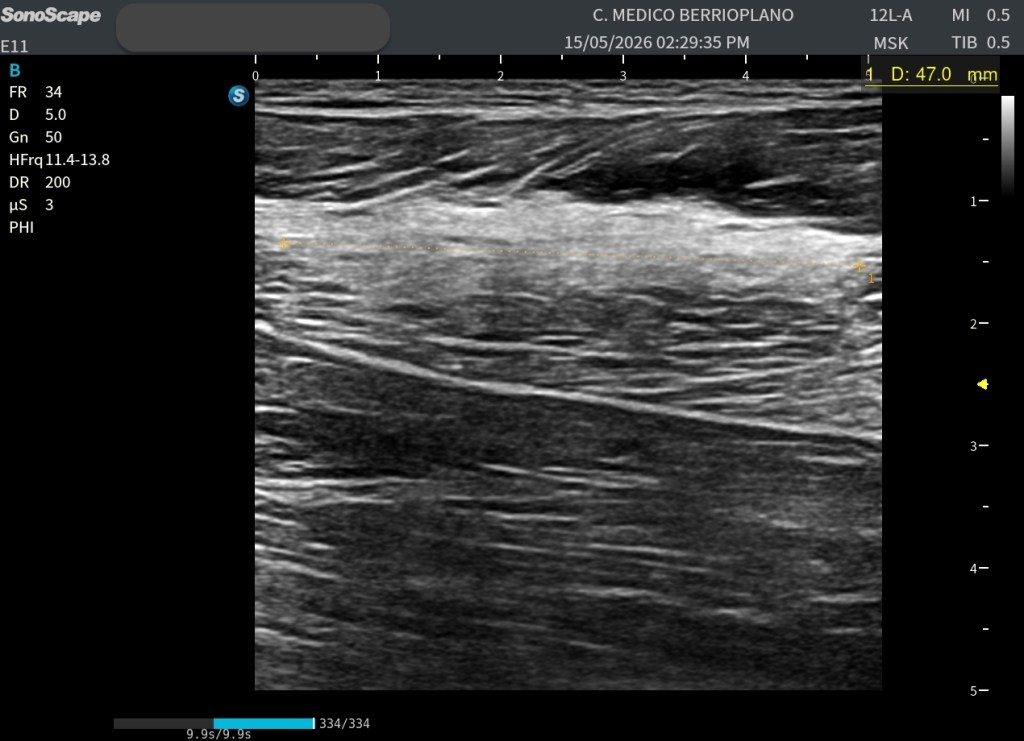
Su aspecto recordaba inmediatamente a una antigua rotura fibrilar reparada, evolucionada hacia un proceso de fibrosis cicatricial.
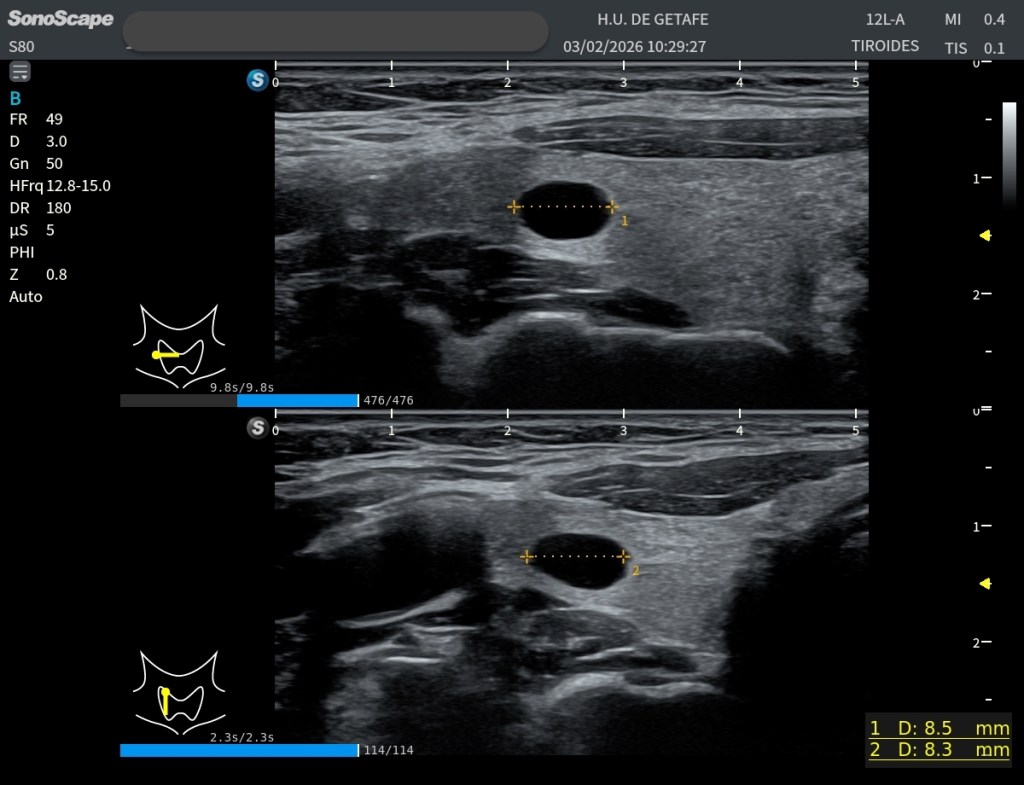
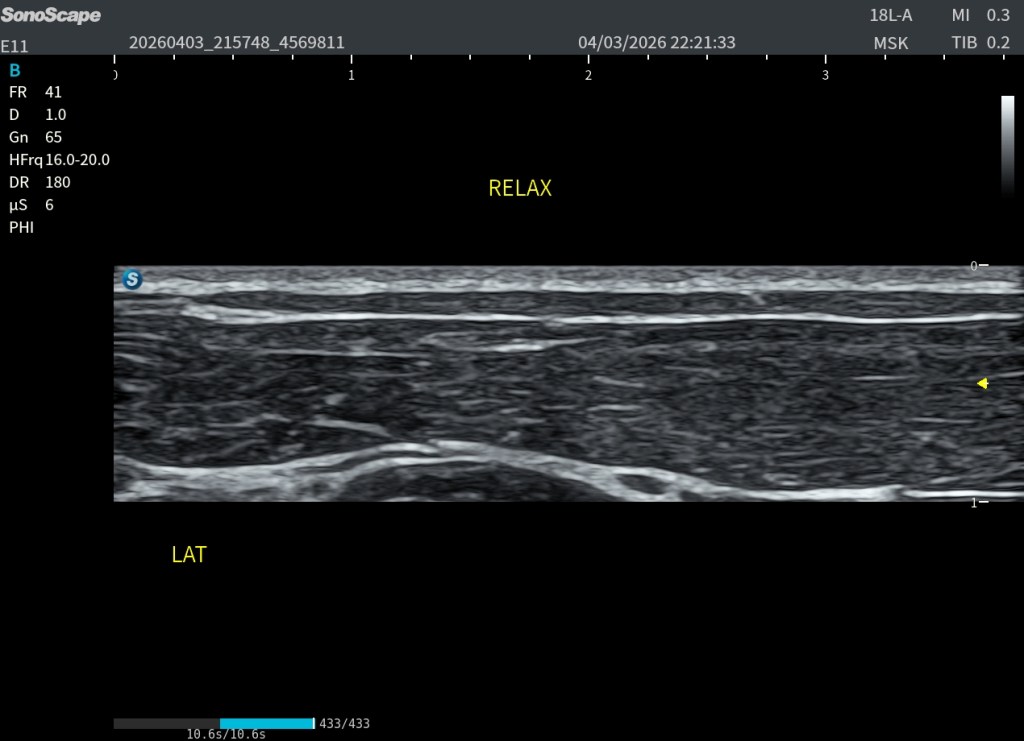
Lo primero, siempre comparar en el Modo B, la zona de sospecha con la zona contalateral, en la imagen ya vemos claremente diferencias:
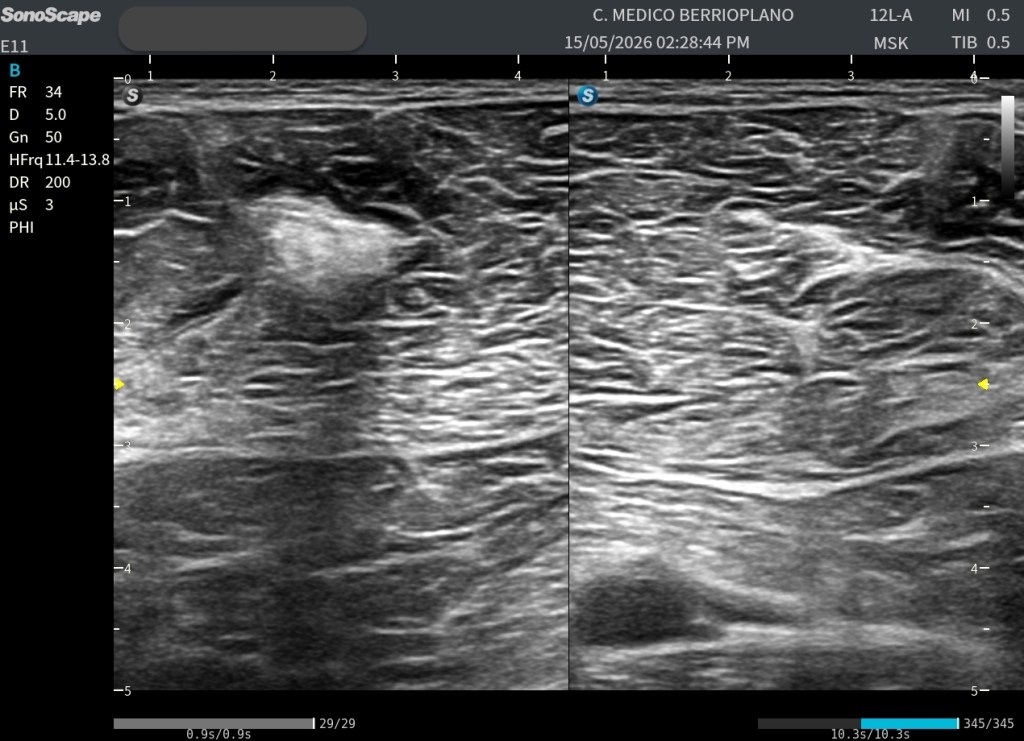
La imagen en escala de grises ya aportaba información relevante. Sin embargo, decidimos añadir una herramienta que cada vez tiene más presencia en la ecografía musculoesquelética: la elastografía de strain:
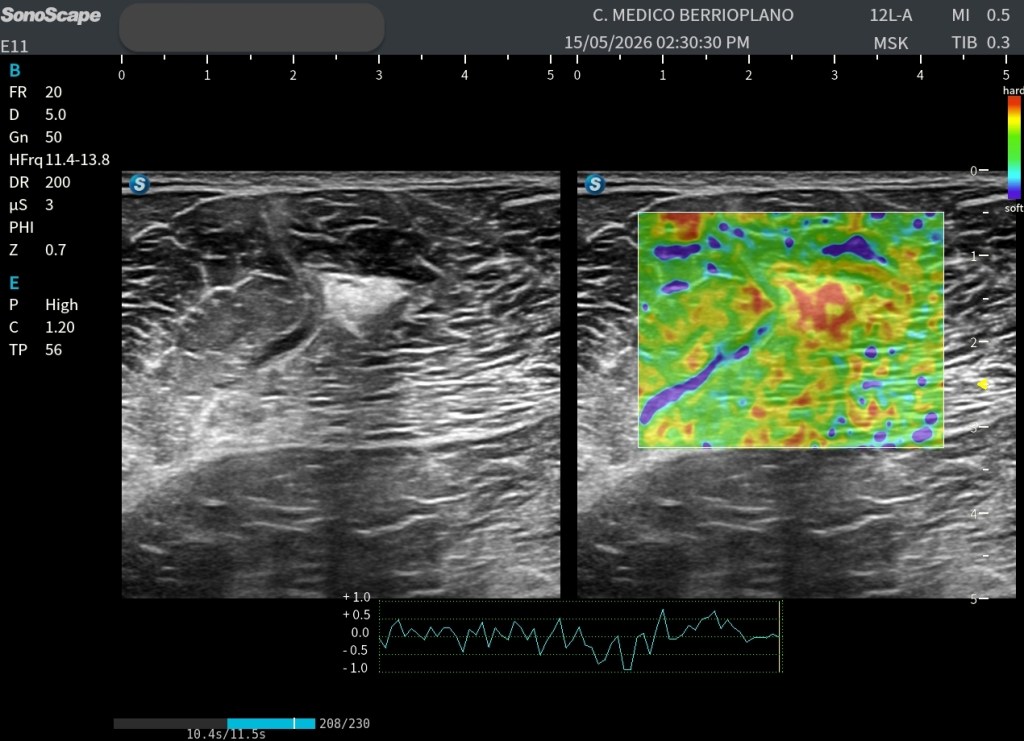
El Elastograma como complemento de la imagen convencional.Clave.
Al activar el elastograma, como el que tienes arriba, sin utilizar ratios ni mediciones cuantitativas, adquirió una dimensión completamente diferente. La estructura hiperecogénica destacaba de forma evidente respecto al tejido muscular circundante. El mapa elastográfico mostraba una distribución de colores claramente distinta a la del músculo sano adyacente, sugiriendo una marcada diferencia en las propiedades mecánicas del tejido.
Este es precisamente uno de los grandes valores del elastograma basal: permitir una rápida identificación visual de zonas cuya elasticidad difiere significativamente de la normalidad.
Aunque frecuentemente se asocia la elastografía a la obtención de ratios o mediciones cuantitativas, la realidad es que el propio mapa de elasticidad ya aporta una enorme cantidad de información cuando se interpreta correctamente y siempre en correlación con la imagen ecográfica convencional.
Correlación entre la imagen anatómica y el elastograma
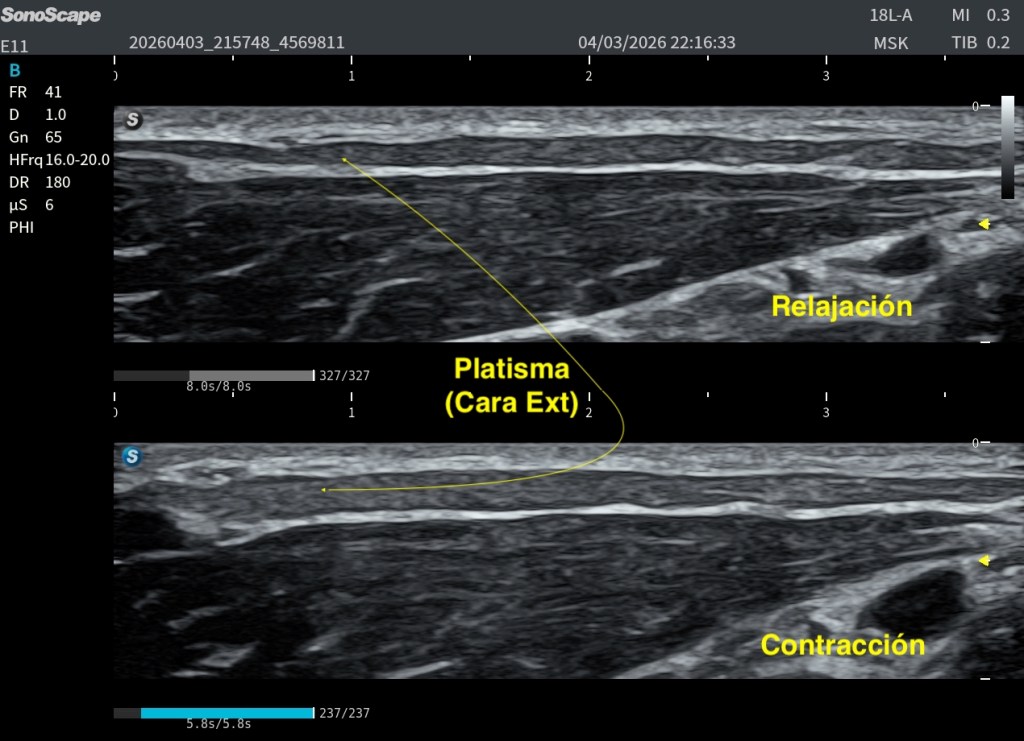
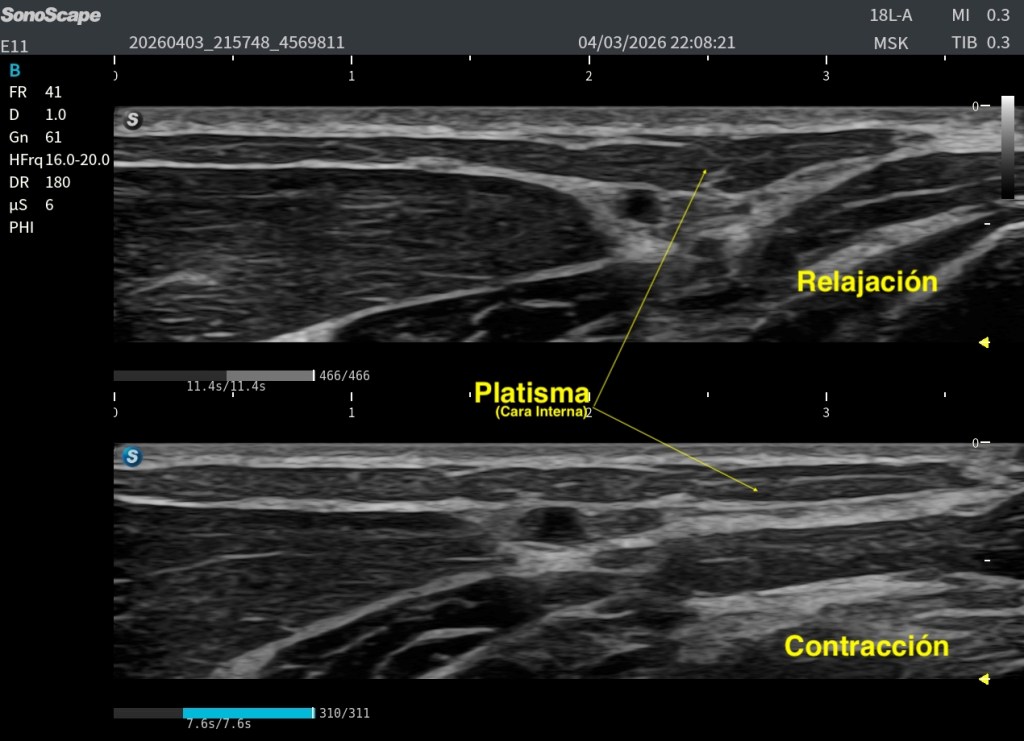
Las imágenes obtenidas permiten valorar la lesión desde diferentes perspectivas. Disponemos tanto de cortes axiales como de cortes longitudinales, donde la estructura hiperecogénica puede identificarse claramente dentro del espesor muscular.
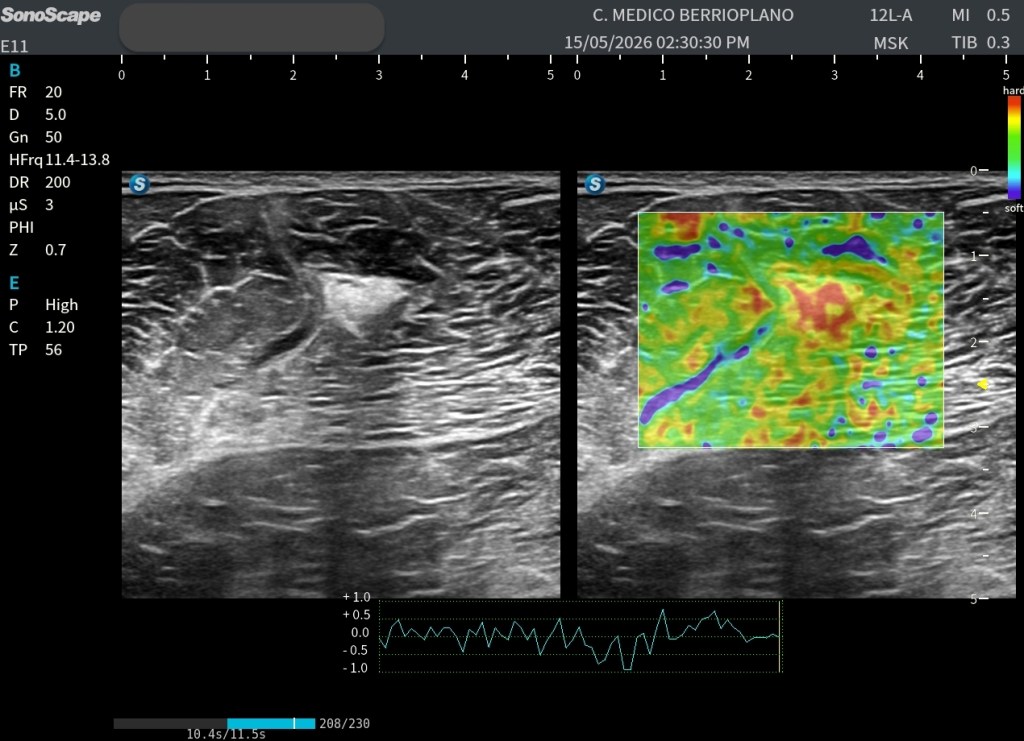
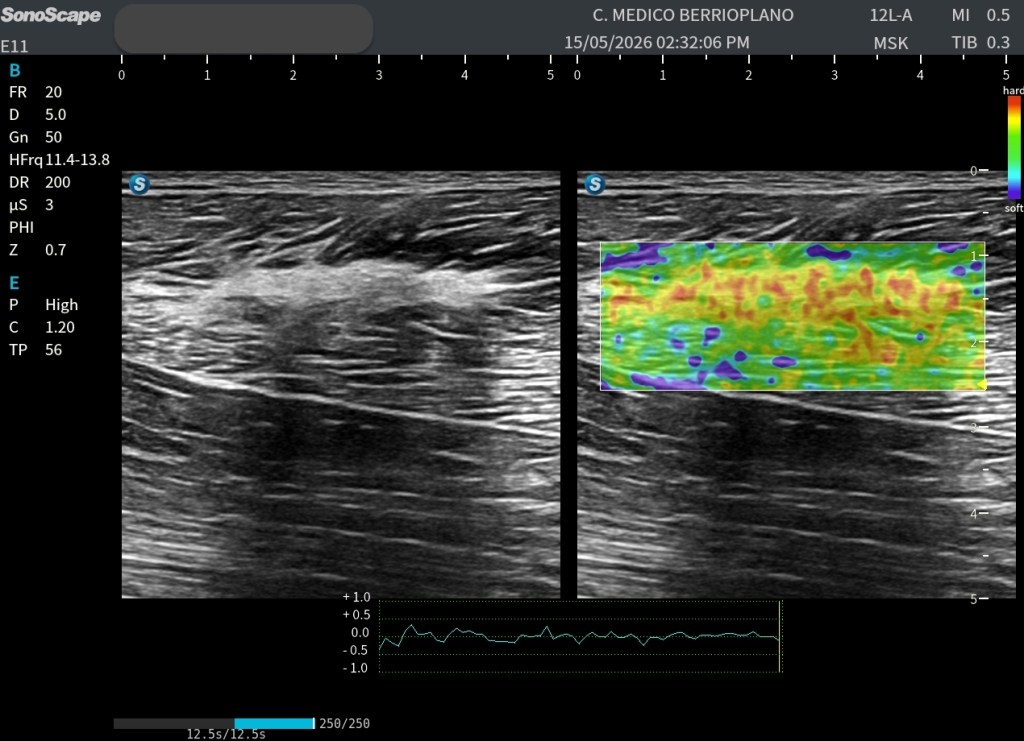
Especialmente interesante resulta la comparación entre la zona aparentemente normal y la zona patológica. Esta comparación permite apreciar cómo la arquitectura muscular habitual se altera en el área de la lesión, repito esto ya que es clave.
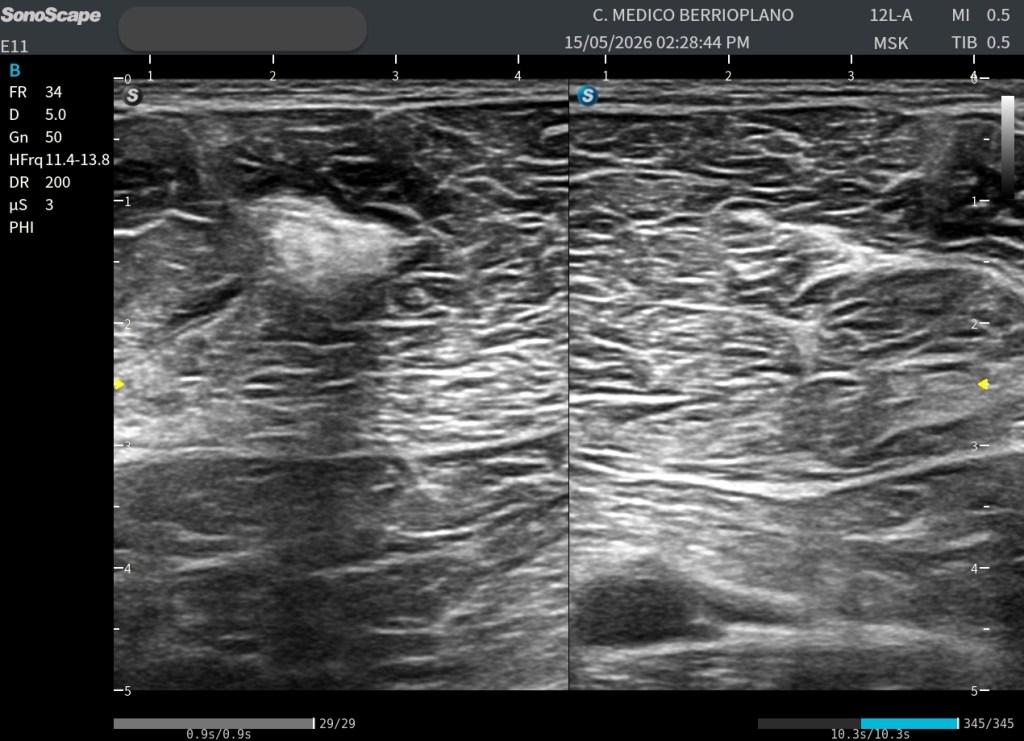
En el tejido sano se observa el patrón fibrilar muscular habitual, con una distribución homogénea de ecos y una elasticidad relativamente uniforme. Sin embargo, en la región patológica aparece una estructura claramente diferenciada tanto desde el punto de vista morfológico como mecánico.
La imagen en modo B ya pone de manifiesto esta alteración estructural mediante el aumento de ecogenicidad de la zona. No obstante, al activar el elastograma, la diferencia se vuelve todavía más evidente. La región sospechosa presenta un comportamiento mecánico distinto al del músculo circundante, delimitándose visualmente respecto al tejido sano y facilitando la identificación de la lesión.
Este es uno de los aspectos más interesantes de la elastografía de strain: su capacidad para resaltar diferencias tisulares que ya existen anatómicamente, pero que pueden hacerse mucho más evidentes cuando se analizan desde el punto de vista de la elasticidad.
Por ello, más que sustituir a la ecografía convencional, el elastograma debe entenderse como una herramienta complementaria que añade información funcional al estudio morfológico, ayudando a localizar, caracterizar y documentar alteraciones tisulares de forma rápida y visual.
La importancia de conocer los parámetros técnicos, imprescindible.
En muchas ocasiones se presta atención exclusivamente al resultado visual del elastograma, olvidando que una correcta interpretación exige conocer los parámetros técnicos con los que se ha adquirido. Los parámetros son clave en una buena técnica, es obligatorio conocerlos para documentar todo con rigurosidad. Son dependientes del operador de forma exclusiva. En el cuadro amarillo están marcados y en el texto, explicados:
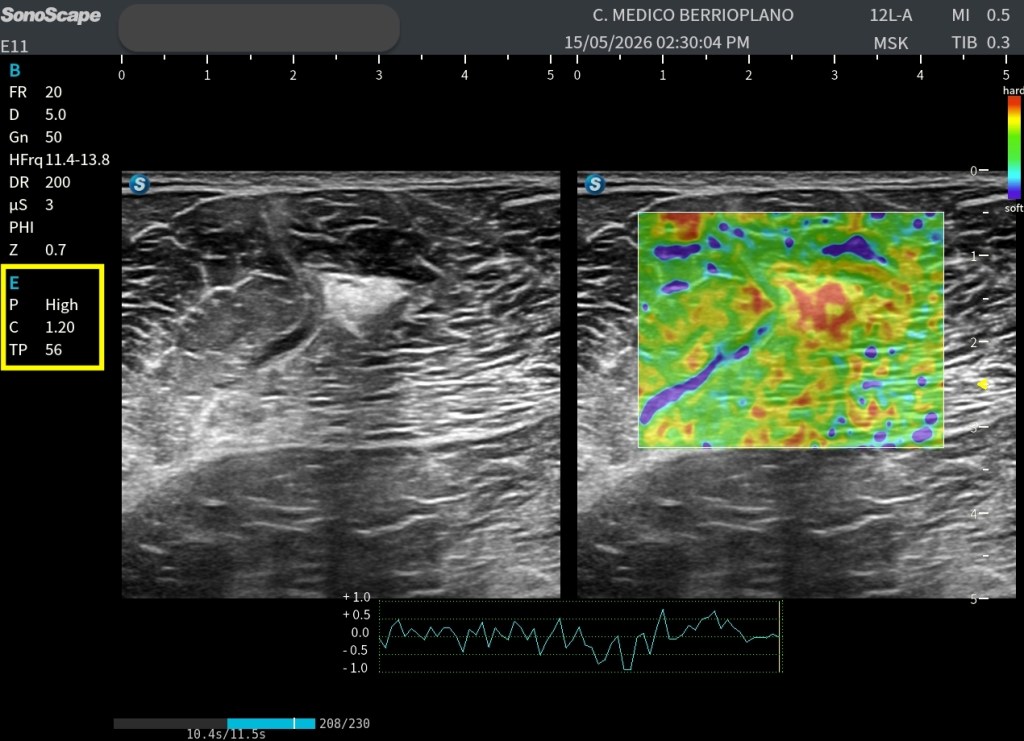
En este caso concreto se emplearon los siguientes ajustes:
Persistencia (P): High
La persistencia determina el grado de suavizado temporal del elastograma.
Un nivel alto de persistencia realiza un promedio de múltiples fotogramas consecutivos, reduciendo el ruido y estabilizando el mapa de colores.
El resultado es una imagen más uniforme, más estable y menos susceptible a pequeñas variaciones producidas por el movimiento o por cambios mínimos en la compresión.
Aunque una persistencia elevada puede disminuir ligeramente la sensibilidad para detectar cambios rápidos, en lesiones fibróticas suele proporcionar una representación más fiable y fácil de interpretar.
Contraste (C): 1,20
El contraste controla la separación visual entre tejidos con diferente elasticidad.
Valores elevados aumentan las diferencias entre colores, mientras que valores bajos generan transiciones más suaves.
El valor utilizado, 1,20, representa un ajuste moderado que permite resaltar diferencias de elasticidad sin exagerarlas artificialmente, algo especialmente importante cuando se estudian procesos cicatriciales o fibróticos.
Transparencia (TP): 56
La transparencia regula el grado de mezcla entre el mapa elastográfico y la imagen anatómica en modo B.
Cuando la transparencia es baja predominan los colores del elastograma.
Cuando es alta, adquiere más protagonismo la anatomía convencional.
Con un valor de 56%, se consigue un equilibrio muy adecuado para la exploración musculoesquelética, permitiendo visualizar simultáneamente la arquitectura fibrilar del músculo y la distribución de elasticidad del tejido estudiado.
Conviene recordar que estos parámetros no tienen significado clínico directo.
No indican si una lesión es más grave o menos grave, ni permiten establecer un diagnóstico por sí mismos.
Su importancia es fundamentalmente técnica y radica en garantizar una representación adecuada del tejido estudiado.
Lo realmente relevante durante la interpretación del elastograma es analizar:
- El patrón de colores.
- La homogeneidad o heterogeneidad del mapa elastográfico.
- La comparación con el tejido sano adyacente.
- La calidad de la adquisición.
- La correlación con la imagen ecográfica convencional.
¿Qué mostraba el elastograma?
La lesión presentaba un patrón claramente heterogéneo.
Las áreas rojo-anaranjadas correspondían a zonas de mayor rigidez, compatibles con tejido fibrótico más maduro.
Las áreas verdes representaban regiones de elasticidad intermedia.
Algunas pequeñas zonas azuladas o violáceas sugerían regiones relativamente más blandas.
Este comportamiento elastográfico podría ser compatible con una cicatriz muscular en fase de remodelación, donde conviven áreas de fibrosis consolidada con otras zonas que mantienen características mecánicas diferentes.
Desde el punto de vista práctico, el elastograma permite identificar de manera inmediata que la estructura hiperecogénica observada en modo B presenta una elasticidad distinta a la del músculo sano adyacente, reforzando la sospecha de encontrarnos ante una alteración tisular real y no ante una simple variación anatómica.
La correlación clínica sigue siendo imprescindible
Por supuesto, ningún elastograma debe interpretarse de forma aislada.
La historia clínica, los antecedentes traumáticos, la exploración física y el resto de hallazgos ecográficos continúan siendo fundamentales para alcanzar una conclusión diagnóstica adecuada.
En este caso concreto, el paciente no acudía por una sospecha de lesión muscular ni existía inicialmente una orientación clínica dirigida hacia esta región anatómica. Por ello, el hallazgo adquiere especial interés como descubrimiento incidental durante una exploración realizada por otro motivo.
La documentación adecuada por parte del EcoTSID de este tipo de hallazgos resulta fundamental para proporcionar al radiólogo toda la información disponible y permitir que, si lo considera necesario, pueda ampliar el estudio o solicitar pruebas complementarias.
Conclusión
Este caso demuestra cómo una lesión hallada de forma casual puede adquirir una nueva dimensión cuando se estudia mediante elastografía de strain.
Más allá de ratios, índices o mediciones cuantitativas, el elastograma basal constituye una herramienta extraordinariamente útil para localizar, caracterizar y documentar estructuras patológicas en ecografía musculoesquelética.
La combinación de cortes axiales y longitudinales, junto con la comparación entre tejido sano y tejido patológico, permite comprender mejor tanto la extensión anatómica de la lesión como su comportamiento mecánico.
El elastograma aporta una información visual inmediata que facilita la detección de alteraciones tisulares y ayuda a reforzar los hallazgos observados en modo B.
Además, conviene recordar que la elastografía de strain está disponible en la mayoría de los ecógrafos actuales, formando parte del equipamiento estándar de numerosos equipos clínicos. Aunque la elastografía Shear Wave sigue siendo una tecnología más avanzada y no siempre disponible, el elastograma basado en strain puede utilizarse en la práctica diaria sin necesidad de equipamiento específico adicional.
Por ello, conocer sus fundamentos, comprender sus parámetros técnicos y aprender a interpretar correctamente sus patrones visuales puede aportar información complementaria de gran valor en la evaluación de múltiples patologías musculoesqueléticas.
Porque, en ocasiones, una simple imagen de colores no solo confirma lo que sospechamos en modo B, sino que nos permite comprender mejor el comportamiento mecánico real del tejido que estamos observando.
Gracias por tanto, querido Profesor, Javier Álvarez, Dr. en Fisioterapia, imposible sin usted comprender los entresijos de la ecografía muscular. Gracias querido amigo. Gracias por enseñarnos tanto.